一酸化窒素(NO)合成酵素完全欠損マウスの開発と機能解析
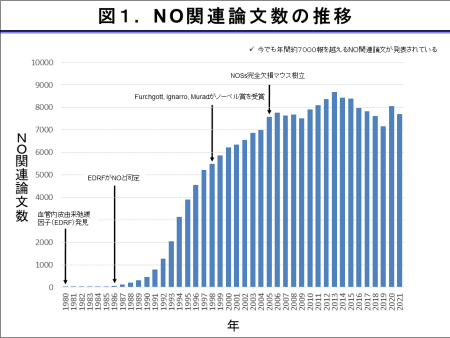
一酸化窒素(nitric oxide: NO)の研究は、1980年のFurchgottらによる血管内皮由来弛緩因子(endothelium-derived relaxing factor: EDRF)の発見を端緒として始まりました。1986年にFurchgott, Iggnaro, Moncadaらがそれぞれ独立してEDRFがNOであることを同定して以来、NOの研究は爆発的に発展しました。NOが血管のみならず全身のほとんどすべての組織・臓器において産生・遊離され多彩な生物活性を発揮していることが明らかにされ、1998年にはNOの発見に貢献したFurchgott, Iggnaro, Muradの3氏にノーベル医学生理学賞が授与されました。EDRFの発見から40年以上が経過した今日においてもNOの研究は世界中で活発に行われており、現在でも毎年7000報を越えるNO関連論文が発表されています(図1)。
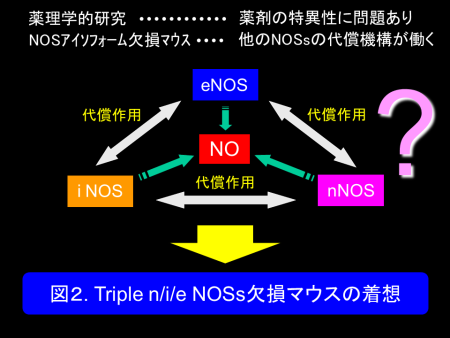
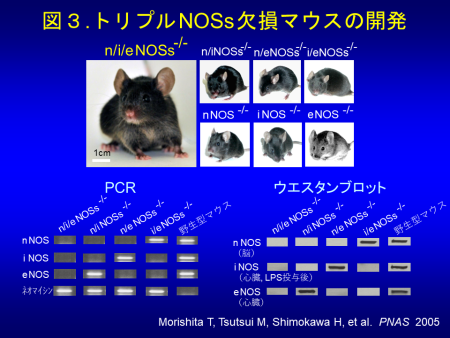
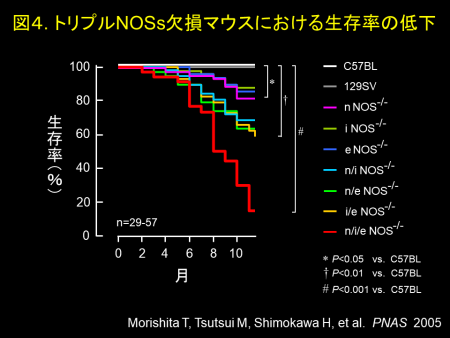
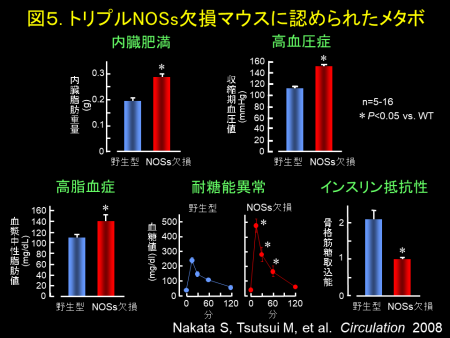
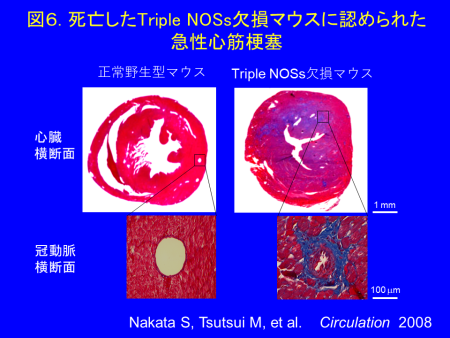
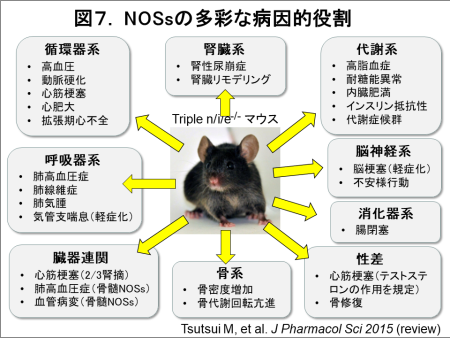
NOはガス状の生理活性物質であり、受容体を介さずに細胞膜を自由に通過して、細胞内でシグナルを伝達します。NO合成酵素(NOS)には、神経型(nNOS)、誘導型(iNOS)、内皮型(eNOS)の3種類の異なったアイソフォームが存在します。従来、生体内におけるNOSsの役割が、非選択的NOSs阻害薬を用いた薬理学的研究やNOSアイソフォーム欠損マウスを用いて広く研究されてきました。しかし、非選択的NOSs阻害薬は様々な非特異的作用を有しており、またNOSアイソフォーム欠損マウスではノックアウトされていない他のNOSによる代償機構が働くため、生体内におけるNOSsの真の役割は未だ十分に解明されていません(図2)。この問題点を克服するために、私達は、3年をかけて、3つのNOSsをすべて欠損させたNOSs完全欠損マウス(triple n/i/eNOSs-/-マウス)を世界に先駆けて開発しました(PNAS 2005)(図3)。この研究は、国際医療福祉大学大学院の下川宏明先生との共同研究です。triple NOSs-/-マウスは、幸運にも胎生致死ではなく誕生しましたが、出生率や生存率は野生型マウスに比して著明に低下していました(図4)。triple NOSs-/-マウスには、高血圧、高脂血症、耐糖能異常、内臓肥満といったメタボリックシンドロームが認められ(図5)、主に自然発症の心筋梗塞で死亡していました(図6)(Circulation 2008)。加えて、私達は、triple NOSs-/-マウスには、循環器系、腎臓系、代謝系、呼吸器系、骨系を含めた様々なシステムに異常が認められることを報告しました(図7)。私達は、NOSsが全身の様々な疾患の成因において重要な役割を果たしていることを明らかにすることが出来ました。私達は、この世界唯一のtriple n/i/eNOSs-/-マウスを用いて、ヒトの病気の成因を詳細に解明し、その知見を臨床に還元して、臨床医学の発展に貢献することを目指して日々研究を行っています。